Calculer la pression partielle d’un gaz, le pourcentage de gaz dans un mélange et la profondeur maximale
Calculer la pression partielle d’un gaz, le pourcentage de gaz dans un mélange et la profondeur maximale
Table des matières
Introduction
L’eau exerçant une pression de 1bar tous les 10 mètres, plus un plongeur descend, plus la colonne d’eau au-dessus pèse sur lui et sur les éléments qu’il transporte dont les gaz.
En plongée sous-marine, la loi de Dalton est utilisée pour calculer la profondeur maximale, la pression partielle d’un gaz ou la pression exercée.
Lors de nos formations il est souvent fait référence en plongée loisirs à la pression partielle d’Oxygène (PpO2 1.4) et au maximum (PpO2 1.6) en plongée sportive, il ne faut pas oublier non plus la narcose induite par la pression partielle d’azote (PpN2) dès 30m environ.
Par exemple, ces calculs vous permettent de :
- Déterminer en fonction de la toxicité d’un gaz la profondeur maximale de son utilisation.
- Retrouver le pourcentage d’un gaz dans un mélange.
- Calculer la pression partielle du gaz à une certaine profondeur.
La loi de Dalton
La loi de Dalton s’applique en physique, dans le domaine de la thermodynamique, elle définit que la pression partielle d’un gaz (PpG) dans un mélange et directement proportionnelle au pourcentage du gaz dans le mélange.
Que dit la loi de Dalton ?
A température constante, dans un mélange de gaz, la pression absolue totale est égale à la somme des pressions partielles qu’aurait chacun des gaz s’il occupait la totalité du volume gazeux.
Selon la loi de Dalton, il est important de noter que...
Un mélange de gaz doit toujours faire 100%, si on augmente ou si l’on diminue le pourcentage d’un des gaz il faudra obligatoirement le remplacer par un autre gaz.
Vous trouverez ci-dessous le glossaire de toutes le abréviations utilisées dans cet article.
- PpO₂ (Pression Partielle d’Oxygène) : Quantité d’oxygène mesurée en bar dans un mélange gazeux sous une pression donnée. (PpO₂ = FO₂ x P.abs)
- FO₂ (Fraction d’Oxygène) : Proportion d’oxygène dans un mélange respiratoire (L’air contient 21 % d’O₂, donc FO₂ = 0,21. Un Nitrox 40 contient 40 % d’O₂, donc FO₂ = 0,40).
- P.abs (Pression Absolue) : Pression totale exercée sur un plongeur, incluant la pression atmosphérique et celle de l’eau. Identique à Pamb.
- Pamb (Pression Ambiante) : Pression totale exercée sur un plongeur, incluant la pression atmosphérique et celle de l’eau. Identique à P.abs.
- PpG (Pression Partielle d’un Gaz) : Pression partielle d’un gaz donné dans un mélange sous une pression absolue spécifique.
- %G (Pourcentage d’un Gaz) : Fraction d’un gaz spécifique exprimée en pourcentage dans un mélange respiratoire.
- P (Pression) : Terme général désignant la force exercée sur une surface, exprimée en bar ou en atm.
- P.m (Pression Manométrique) : Pression mesurée par un manomètre, sans inclure la pression atmosphérique (P.m = P.abs – 1 bar).
- bar : Unité de pression utilisée en plongée, 1 bar ≈ pression atmosphérique au niveau de la mer.
- O₂ (Oxygène) : Gaz essentiel à la respiration, composant environ 21 % de l’air. En plongée, utilisé pur ou en mélange avec d’autres gaz.
- N₂ (Azote) : Gaz inerte constituant environ 78 % de l’air. Peut provoquer la narcose à l’azote en profondeur.
- Autres gaz : Gaz présents en faible quantité dans l’air, comme l’argon, l’hélium (He) utilisé en plongée technique (Trimix, Heliox), et le dioxyde de carbone (CO₂).
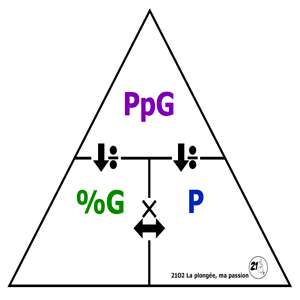
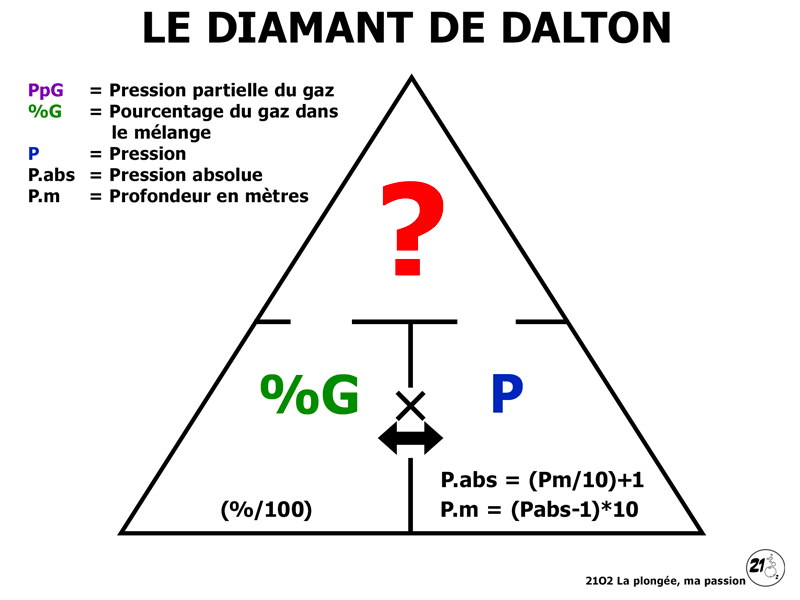
Le diamant de Dalton
Il y a trois formules indispensables en plongée sous-marine, pour les résoudre vous pouvez vous appuyer sur le diamant de Dalton, aux premiers abords cela peut sembler compliqué, mais quand on a compris le principe c’est tout simple, je vous ai recréé le Diamant de Dalton ci-dessous et je vais tenter de vous expliquer le principe.
Comment utiliser le diamant de Dalton
- Pour comprendre et utiliser le diamant de Dalton, il faut s’imaginer cacher une partie du diamant afin d’obtenir la formule permettant de résoudre la partie cachée.
Règle de base de la formule :
- De haut en bas on effectue une DIVISION.
- De gauche à droite et inversement, on effectue une MULTIPLICATION.
- Pression partielle de gaz (PpG).
- Pourcentage de gaz (%G).
- Profondeur (P).
Sortons nos calculatrices

Déterminer la pression absolue en bar quand on connait la profondeur
Pour déterminer la pression absolue (bar) il suffit de diviser la profondeur en mètres (P.m) par dix et d’ay ajouter un.
P.abs = (P.m / 10) + 1
Exemple :
Combien représentent la profondeur absolue d’une plongée à 18 mètres ?
(18/10)+1 = 2.8 bar
Exemple :
Combien représentent la profondeur absolue d’une plongée à 30 mètres ?
(30/10)+1 = 4 bar
Déterminer la profondeur en mètres quand on connait la pression absolue en bar
Pour déterminer la profondeur en mètres quand l’on connait la pression absolue, il suffit de soustraire un à la pression absolue et de multiplier le résultat par dix.
P.m = (P.abs – 1) / 10
Exemple :
Quelle est la profondeur en mètres d’une pression absolue de 3.7 ?
(3.7-1)*10 = 27 mètres
Exemple :
Quelle est la profondeur en mètres d’une pression absolue de 5.2 ?
(5.2-1)*10 = 42 mètres

Déterminer la pression partielle d'un gaz (PpG)
Exemple :
Puis-je plonger à 30 mètres avec de l’air, sachant que je suis un plongeur loisir qui ne désire pas dépasser 1.4 de PpO2 (pression partielle d’oxygène) ?
La réponse est oui, mais pour quelle raison ?
- Commençons d’abord par convertir le pourcentage en centième : (21/100) = 0.21
- Calculons la pression absolue (bar) à 30 mètres : (30/10) + 1 = 4
- Calculons maintenant la pression partielle de gaz : (0.21 * 4) = 0.84
Exemple :
Puis-je plonger à 40 mètres avec du Nitrox 38, sachant que je suis un plongeur sportif et que je ne dois pas dépasser 1.6 de PpO2 (pression partielle d’oxygène) ? La réponse est non, mais pour quelle raison.
- Commençons d’abord par convertir le pourcentage en centième : (38/100) = 0.38
- Calculons la pression absolue (bar) à 30 mètres : (40/10) + 1 = 5
- Calculons maintenant la pression partielle de gaz : (0.38 * 5) = 1.9

Déterminer le pourcentage d'un gaz (%G)
Exemple :
Quel est le pourcentage d’oxygène maximal dans mon Nitrox, pour une plongée à 25 mètres en ne dépassant pas une PpO2 de 1.4 ?
- Commençons par convertir la profondeur en pression absolue (bar) : (25/10)+1 = 3.5
- Calculons maintenant le pourcentage de gaz : (1.4 / 3.5) = 0.4
- Terminons par le convertir en pourcentage : (0.4*100) = 40%
Exemple :
Quel est le pourcentage d’oxygène maximal dans mon Nitrox, pour une plongée à 45 mètres en ne dépassant pas une PpO2 de 1.4 ?
- Commençons par convertir la profondeur en pression absolue (bar) : (45/10)+1 = 5.5
- Calculons maintenant le pourcentage de gaz : (1.4 / 5.5) = 0.25
- Terminons par le convertir en pourcentage : (0.25*100) = 25%

Déterminer la profondeur maximale (P)
Exemple :
Je transporte avec moi de l’air contenant 21% d’oxygène, sachant que je ne désire pas dépasser une PpO2 de 1.4, à quelle profondeur puis-je plonger au maximum ?
- Commençons d’abord par convertir le pourcentage en centième : (21/100) = 0.21
- Calculons maintenant la profondeur maximale (bar) : (1.4/0.21) = 6.66 bar
- Terminons par le convertir en pourcentage : (6.66-1)*10 = 56.6m
Exemple :
Je transporte avec moi un bloc de déco. à 80% d’oxygène, sachant que je ne désire pas dépasser une PpO2 de 1.6, à quelle profondeur puis-je commencer ma décompression à l’oxygène ?
- Commençons par convertir le pourcentage en centième : (80/100) = 0.8
- Calculons maintenant la profondeur maximale (bar) : (1.6/0.8) = 2 bar
- Terminons par le convertir en pourcentage : (2-1)*10 = 10m
Exemple :
Je transporte avec moi un bloc de déco. à 100% d’oxygène, sachant que je ne désire pas dépasser une PpO2 de 1.6, à quelle profondeur puis-je commencer ma décompression à l’oxygène ?
- Commençons par convertir le pourcentage en centième : (100/100) = 1
- Calculons maintenant la profondeur maximale (bar) : (1.6/1) = 1.6 bar
- Terminons par le convertir en pourcentage : (1.6-1)*10 = 6m

Tentons des démontrer la loi de Dalton
Je vais tenter en tant que commun des mortels de vous expliquer par des exemples, ce que veut dire la loi de Dalton.
Dans un mélange de gaz, par exemple l’air que nous respirons, la pression de l’air est égale à la somme des pressions partielles des gaz contenus dans cet air.
Tentons de démonter cette loi. Il suffirait d’additionner les pressions partielles des gaz et le résultat devrait être égal à la pression absolue en bar.
Loi de Dalton au bord de la mer :
Imaginons que nous sommes au bord de la mer, donc à 0 mètre avec de l’air dans une bouteille, si nous calculons la pression de l’air, nous devrions arriver à un résultat de 1.
Hé, Dalton, tu as pas dis que le résultat devrait être le même ? 0 est pas égal à 1, je ne comprends pas… C’est normal, Christian, tu dois d’abord le convertir en pression absolue (bar) puis faire le calcul.
Comme sur l’image à gauche, l’air est composé de 21% d’oxygène, de 78% d’azote et d’environ 1% de gaz rares.
- Commençons par convertir la profondeur de 0m en pression absolue : (0/10)+1 = 1 bar
- Calculons maintenant les pressions partielles :
Pour rappel, PpG = (%G * P)
– Oxygène : (21/100)*1 = 0.21
– Azote : (78/100)*1 = 0.78
– Autres gaz : (1/100)*1 = 0.01 - Pour terminer, calculons la pression totale des gaz :
0.21+0.78+0.01 = 1
Loi de Dalton à 40 mètres :
Imaginons que nous sommes à 40 mètres de profondeur avec de l’air dans une bouteille, si nous calculons la pression de l’air, nous devrions arriver à un résultat de 5 bar.
- Commençons par convertir la profondeur de 40m en pression absolue : (40/10)+1 = 5 bar
- Calculons maintenant les pressions partielles (Pour rappel, PpG = (%G * P)) :
– Oxygène : (21/100)*5 = 1.05
– Azote : (78/100)*5 = 3.9
– Autres gaz : (1/100)*5 = 0.05 - Pour terminer, calculons la pression totale des gaz :
1.05+3.9+0.05 = 5 - La pression totale des gaz est donc équivalente à la profondeur en bar (5 = 5).
Les articles suivants traitent d'un sujet en lien avec cet article

Quel est le pourcentage maximum d’O2 (oxygène) que je peux mettre dans une bouteille de plongée qui n’est pas Oxyclean

La narcose à l’azote souvent appelée l’ivresse des profondeurs est directement liée à la pression partielle d’azote, mais pourquoi…

La maladie de décompression (MDD) et l’accident de décompression (ADD) simplement expliqué
Si nous remontons trop vite lors d’une plongée la pression chute trop rapidement, dès lors les mécanismes naturels de dégazage sont surchargés et ne peuvent pas effectuer le dégazage au travers de la respiration et c’est exactement le sujet de cet article…
Views: 8884




bonjour,
on entend souvent dire que la toxicité de l’O² est de 1.4 voire 1.6. Je cherche à comprendre comment cette PP o² a été calculée? Sachant que l’air est composé grosso modo de 20% O² et 80% N² je pensais que la PP O² était de 2 Bars.
suis preneur d’infos
merci à vous
pascal
Bonjour,
Désolé pour ma réponse un peu tardive, mais répondre à cette question prends pas mal de temps en recherche afin de tenter de ne pas trop dire de bêtises. J’en ai aussi profité pour écrire un glossaire des abréviations dans mon article car ça manquait furieusement.
⠀
Avant de tenter de te répondre Marko je vais corriger une petite erreur dans ta question, l’air contient 21% d’oxygène pour 78% d’azote, le reste de 1% sont des gaz rares, il est de coutume de ne pas toujours compter les gaz rares dans le cas de plongée loisirs (sans décompression), nous calculons souvent 21%/79% pour simplifier les choses.
⠀
Maintenant je vais tenter de répondre à ta question initiale.
La toxicité de l’oxygène a été signalée par Priestley (1775) puis par Lavoisier (1785). Elle prédomine sur l’appareil respiratoire pour des pressions partielles inférieures à 2 bars (Seiler,1881) et sur le système nerveux pour les pressions supérieures à 3 bars (Paul Bert -1878). Paul Bert en (1878), a observé des convulsions chez des animaux exposés à des pressions élevées d’oxygène. Au début du XXe siècle, John Scott Haldane a approfondi ces recherches, influençant les premières tables de plongée. Pendant la Seconde Guerre mondiale, la Royal Navy et la US Navy ont mené des tests sur les plongeurs utilisant des recycleurs à oxygène pur, confirmant que des PPO2 supérieures 1,6 bar provoquaient des convulsions. Dans les années 1960 à 1970 environ, des études en caisson hyperbare ont quantifié ce seuil, et la NOAA (National Oceanic and Atmospheric Administration) et la Diving Medical Advisory Committee (DMAC) ont ensuite fixé des limites opérationnelles sûres, adoptées par les agences de plongée (PADI, TDI, SDI, SSI, etc.).
⠀
Les expérimentations militaires et médicales ont montré qu’à une PPO2 au dessus de 1,6 bar, des convulsions pouvaient survenir sans signes précurseurs, rendant cette valeur critique pour la sécurité.
⠀
La loi de Dalton stipule que la pression partielle d’un gaz dans un mélange est donnée par :
PPO2 = FO2 × P.abs
⠀
La Fo2 est la fraction d’oxygène dans le mélange respiré et P.abs la pression ambiante en bar.
– PPO2 : (Pression Partielle d’Oxygène, en bar)
– FO2 : (Fraction d’Oxygène dans le mélange, sans unité)
– P.abs : (Pression Ambiante, en bar)
Exemple : avec un Nitrox 40% (FO2 = 0,40), une PPO2 de 1,6 bar est atteinte à 40 mètres de profondeur (5 bar absolus).
⠀
Pour minimiser les risques, les études ont défini :
– 1,6 bar comme limite maximale acceptable pour des expositions courtes.
– 1,4 bar comme seuil opérationnel en plongée loisirs et sportive.
– 0,5 bar comme seuil de sécurité pour des expositions prolongées (plongée technique et à saturation).
⠀
Exemple de calcul réeel :
Si un plongeur respire du Nitrox 40 (PPo2 = 0,40) à 40 mètres (P.abs = 5 bar) le calcul sera
(FO2 040 x 5) = 2 bar
⠀
Danger ! Cette valeur dépasse la limite de 1,6 bar, donc un risque élevé de convulsions existe.
L’application de cette formule est essentielle pour planifier des plongées sécurisées ou de décompression à l’oxigène elle permet d’éviter la toxicité de l’oxygène.
⠀
En Français
Pour creuser un peu plus le sujet, je te propose de lire le livre suivant en Français
« Le guide de la plongée Nitrox et Trimix » de Pascal BERNABE et François BRUN aux éditions « gap » est une mine d’or sur le sujet.
⠀
En Englais
« NOAA Diving Manual » (National Oceanic and Atmospheric Administration)
« The Physiology and Medicine of Diving 4th Edition » de Peter Bennett & David Elliott
« The Oxygen Revolution, Third Edition: Hyperbaric Oxygen Therapy (HBOT) » The Definitive Treatment of Traumatic Brain Injury (TBI) & Other Disorders
Merci beaucoup pour cet article qui m’a permis de me rafraîchir un peu la mémoire…
Je me permets de signaler une petite erreur qui s’est glissée dans le troisième exemple de calcul de la profondeur maximale avec le bloc de déco à 100%.
100/100=1 et non 0 et donc 1.6/1=1.6
Bonjour Nathaniel,
c’est corrigé, merci pour cette rectification et content que mon article a pu aider, je les écrits pour mon apprentissage et ma mémorisation puis les publies en pensant pouvoir un jour aider qqn à réviser, le but est atteint.
Cordialement
Christian
Bonjour
Cet article est très interressant, merci à toi de nous le partager, néanmoins il me semble qu’une petite erreur c’est glissée
Dans l’exo « calculer sa profondeur » tu demandes le calcul avec une PpO2 de 1,6 et tu réalises le calcul avec une PpO2 de 1,4.
Peut-être que c’est moi qui n’est pas compris.
Encore merci pour toutes ces informations
Chris
Bonjour,
Vous avez tout à fait raison, l’erreur est corrigée.
Je vous remercie pour votre message. Je suis heureux que mon article vous ait été utile. Je les écris souvent lors de mes apprentissages en pensant que le contenu pourrait servir à quelqu’un un jour. Merci pour votre retour, cela m’encourage à continuer.
Cordialement,
Christian